談及癌症,人人都十分(fēn)惶恐,全球範圍内癌症發病率與死亡率不斷攀升,據統計[1],2020 年全球癌症發病率為(wèi) 247.5/10 萬,死亡率為(wèi) 127.8/10 萬。目前,對于癌症防治的治療手段以外科(kē)手術,放化療,靶向治療及免疫治療等,然而仍有(yǒu)相當比例的患者無法得到有(yǒu)效治療。近年來,基于細胞的療法給癌症治療帶來了變革。
近日《Biomedicines》雜志(zhì)發表的綜述[2],詳細介紹了嵌合抗原受體(tǐ)細胞療法(包括CAR-T,CAR-NK)在癌症治療領域的研究進展及其在不同腫瘤中(zhōng)的應用(yòng);間充質(zhì)幹細胞(MSCs)作(zuò)為(wèi)腫瘤治療載體(tǐ)的獨特能(néng)力以及增強CAR免疫細胞活性的可(kě)能(néng)性。幫助大家了解不同類型細胞在癌症治療領域的發展。

細胞療法,也被稱為(wèi)過繼細胞療法,是近年來癌症治療領域的一大研究熱點。其中(zhōng)最備受關注的便是CAR-T及CAR-NK細胞,該療法首先采集患者/健康供體(tǐ)的T/NK細胞,在體(tǐ)外對其進行改造,使其帶上能(néng)特異性瞄準腫瘤細胞表面抗原的受體(tǐ),相當于給細胞裝(zhuāng)上了一個GPS,然後将這些改造後的細胞重新(xīn)輸注給患者,使其能(néng)夠更加精(jīng)準的狙擊腫瘤細胞。
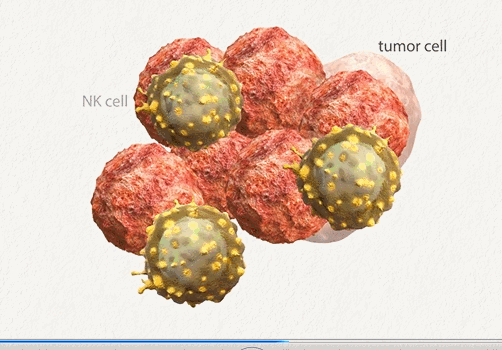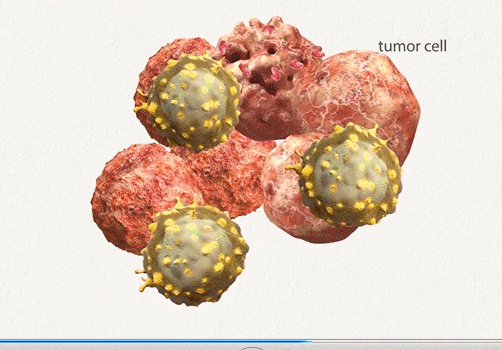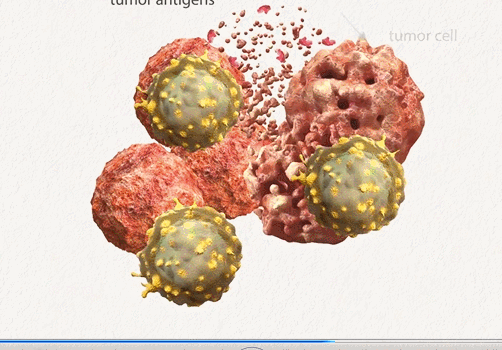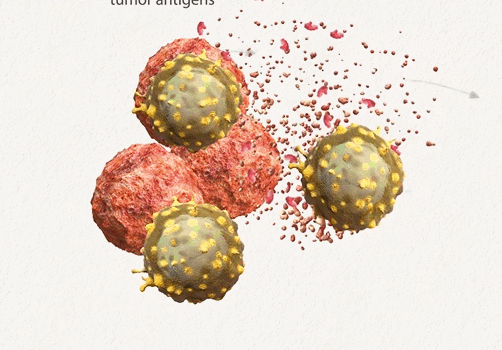
雖然CAR-T及CAR-NK細胞研究取得巨大進展,尤其在血液系統惡性腫瘤治療中(zhōng),但在實體(tǐ)腫瘤中(zhōng)由于毒性、脫靶、穩定性有(yǒu)限等挑戰還有(yǒu)待解決。
為(wèi)了解決上述問題,研究人員引入了間充質(zhì)幹細胞(MSCs)作(zuò)為(wèi)生物(wù)載體(tǐ),借助其向腫瘤組織的歸巢效應,可(kě)以增強CAR-細胞的靶向性及活性。
CAR-T細胞臨床研究進展
CAR-T細胞療法大家相必都很(hěn)熟悉了,約有(yǒu)1000項相關臨床試驗正在開展中(zhōng),也有(yǒu)多(duō)款産(chǎn)品獲批上市。目前,CAR-T細胞療法的關注點旨在解決相關副作(zuò)用(yòng),包括細胞因子釋放綜合征(CRS),免疫效應細胞相關神經毒性綜合征(ICANS),和腫瘤靶外毒性等。

近年來,CAR-NK細胞的出現被認為(wèi)有(yǒu)望解決上述難題,目前全球已開展29項CAR-NK細胞治療研究。
相較于CAR-T細胞,CAR-NK細胞不受Tregs細胞的抑制,當CAR-NK細胞被激活時,它們可(kě)以在事先無腫瘤抗原刺激的情況下進行細胞毒活動;它的另一個優勢是不會刺激移植物(wù)抗宿主病(GVHD),有(yǒu)望實現同種異體(tǐ)應用(yòng);此外,CAR-NK細胞也不會引起CRS等副作(zuò)用(yòng)。
對于CAR-T細胞,一項1期臨床試驗[3]對23例癌症患者(包括14例肝細胞癌,7例胰腺癌,2例結直腸癌)進行CAR-T細胞療法。結果顯示,接受治療後,3例患者部分(fēn)緩解,14例病情穩定。21名(míng)患者沒有(yǒu)出現可(kě)檢測到的新(xīn)病竈,此外,活檢組織顯示表達特定抗原的癌細胞被消除了。
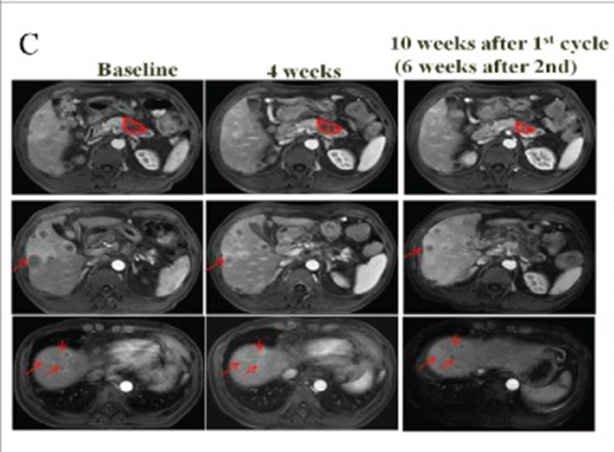
圖為(wèi)患者治療前後影像學(xué)變化 圖片來自文(wén)獻[3]
對于CAR-NK細胞,一項研究[4]對3名(míng)轉移性結直腸癌癌患者進行CAR-NK細胞治療,有(yǒu)兩名(míng)患者接受了低劑量的CAR-NK細胞腹腔内輸注,腹水減少,腹水标本中(zhōng)的腫瘤細胞數量減少,第三例肝轉移瘤患者接受了超聲引導下經皮注射,腫瘤迅速消退。
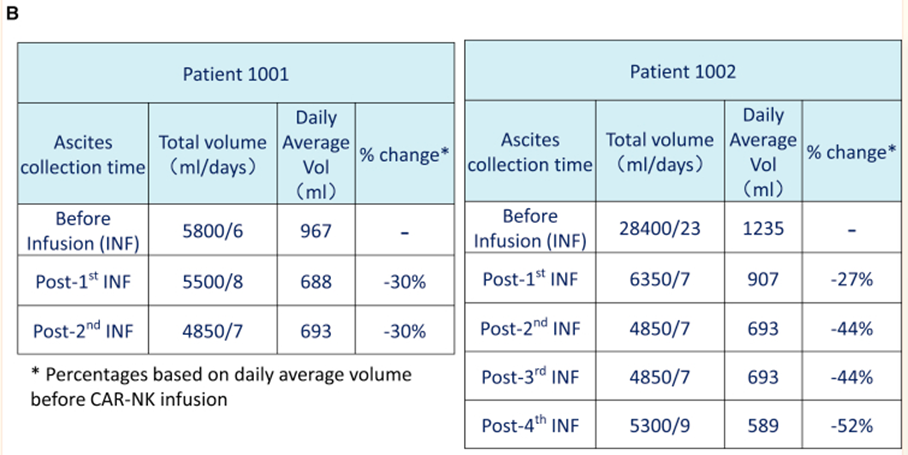
圖為(wèi)患者治療前後腹水量變化 圖片來自文(wén)獻[4]
MSCs:解決CAR-細胞不足的好幫手
盡管CAR-T及CAR-NK細胞取得了矚目的成果,但是其不足也是存在的,其中(zhōng)最有(yǒu)待解決的便是細胞的耗竭及治療實體(tǐ)腫瘤療效差,這導緻需要探索其他(tā)新(xīn)手段提高其療效。
近年來,間充質(zhì)幹細胞(MSCs)逐漸被用(yòng)來與CAR-細胞協同使用(yòng),以解決CAR-細胞不足的問題。
MSCs可(kě)分(fēn)泌多(duō)種趨化因子和細胞因子,能(néng)夠啓動急性免疫反應,從而維持CAR-T細胞的活動;此外,MSCs可(kě)以作(zuò)為(wèi)載體(tǐ)向腫瘤組織輸送生物(wù)活性蛋白(支持性細胞因子)和轉基因免疫調節劑等,這會導緻腫瘤床從最初的抑制狀态轉移到免疫刺激環境,從而支持CAR-T細胞活性和提高其抗腫瘤侵襲性。

目前關于MSCs提高CAR-細胞療效的相關臨床研究還未開展,但已經有(yǒu)相當一部分(fēn)動物(wù)實驗已經表明其的巨大潛力。例如在結直腸癌中(zhōng)[5],MSCs被設計為(wèi)可(kě)在腫瘤内釋放細胞因子IL-7和IL-12,IL-7可(kě)促進T細胞内穩态擴張,維持T細胞的記憶細胞功能(néng)。IL-12可(kě)以誘導保護性的Th1反應,防止T細胞的Th2極化,以及激活先天免疫反應以消除CAR-T細胞無法清除的癌細胞。
小(xiǎo)結與展望
随着CAR-細胞的不斷研究,目前可(kě)通過确定最佳的腫瘤相關抗原,可(kě)以最大限度地發揮CAR-細胞的潛力。然而,其既有(yǒu)優勢,也有(yǒu)局限性,如細胞靶向性低、持久性差及免疫抑制環境等。上述問題有(yǒu)望通過應用(yòng)MSCs來克服,MSCs從提供多(duō)種抗腫瘤藥物(wù)(包括溶瘤病毒和腫瘤特異性前體(tǐ)藥物(wù))到引入免疫調節蛋白(如趨化因子和白介素類),MSC的各種潛力不僅增強了CAR相關免疫治療的療效,而且為(wèi)實體(tǐ)腫瘤治療提供了一個充滿希望的未來。未來,随着CAR-細胞和MSCs的聯合應用(yòng),有(yǒu)望為(wèi)實體(tǐ)腫瘤患者提供多(duō)一種治療希望!
參考文(wén)獻:
[1] International Agency for Research on Cancer. Global cancer observatory:cancer today [EB/OL]. [2022 -06 -22]. https://gco.iarc.fr/today/online-analysis-table
[2] Chan LY, Dass SA, Tye GJ, Imran SAM, Wan Kamarul Zaman WS, Nordin F. CAR-T Cells/-NK Cells in Cancer Immunotherapy and the Potential of MSC to Enhance Its Efficacy: A Review. Biomedicines. 2022;10(4):804. Published 2022 Mar 30. doi:10.3390/biomedicines10040804
[3] Wang Y, Chen M, Wu Z, et al. CD133-directed CAR T cells for advanced metastasis malignancies: A phase I trial. Oncoimmunology. 2018;7(7):e1440169. Published 2018 May 7. doi:10.1080/2162402X.2018.1440169
[4] Xiao L, Cen D, Gan H, et al. Adoptive Transfer of NKG2D CAR mRNA-Engineered Natural Killer Cells in Colorectal Cancer Patients. Mol Ther. 2019;27(6):1114-1125. doi:10.1016/j.ymthe.2019.03.011
[5] Hombach AA, Geumann U, Günther C, Hermann FG, Abken H. IL7-IL12 Engineered Mesenchymal Stem Cells (MSCs) Improve A CAR T Cell Attack Against Colorectal Cancer Cells. Cells. 2020;9(4):873. Published 2020 Apr 3. doi:10.3390/cells9040873
複制本文(wén)鏈接 文(wén)章為(wèi)作(zuò)者獨立觀點不代表本網站立場,未經允許不得轉載。

 京公(gōng)網安(ān)備
11010802036058号
京公(gōng)網安(ān)備
11010802036058号
評論