近年來,細胞療法為(wèi)衆多(duō)疾病的再生治療帶來了巨大的希望。最近幹細胞修複大腦損傷的臨床研究方面取得了突破性進展,不過将細胞療法應用(yòng)于大腦損傷的治療結果仍然有(yǒu)待提高。
近日,瑞士科(kē)學(xué)家在國(guó)際期刊《The Neuroscientist》發表相關綜述[1],總結了幹細胞療法的前景及局限性,并提出了五條原則來推進幹細胞療法在大腦損傷修複中(zhōng)的應用(yòng),文(wén)章側重于中(zhōng)風的細胞療法,但同樣也适用(yòng)于其他(tā)腦部疾病。

中(zhōng)風是世界範圍内導緻殘疾和死亡的主要原因,據估計,全球因中(zhōng)風造成的損失超過7210億美元(占全球GDP的0.66%)。從1990年到2019年,中(zhōng)風發病率增加70.0%,因中(zhōng)風死亡人數增加43.0%[2]。
然而,目前對于中(zhōng)風還缺少有(yǒu)效治療手段,迅速修複甚至逆轉中(zhōng)風後腦損傷成為(wèi)一大研究熱點。近年來,随着再生醫(yī)學(xué)的迅猛發展,也給中(zhōng)風後腦損傷修複帶來了希望,然而,中(zhōng)風的異質(zhì)性給幹細胞療法的臨床應用(yòng)帶來了不小(xiǎo)挑戰。因此,上述文(wén)章确定了幹細胞療法在中(zhōng)風治療中(zhōng)的五個主要的限制及未來突破點,并利用(yòng)細胞和基因工(gōng)程領域的最新(xīn)進展提供了相應的解決方案[1]。
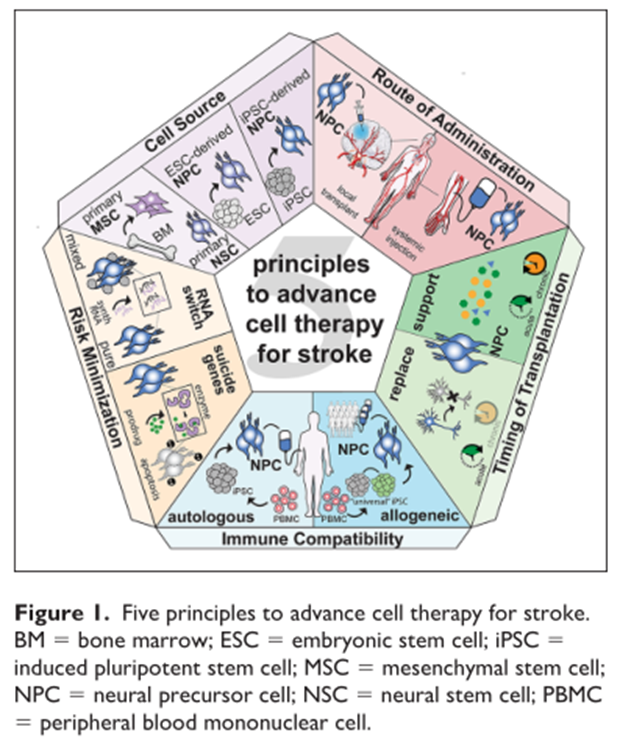
圖片來自文(wén)獻[1]
01 細胞來源
各種來源的幹細胞均被認為(wèi)可(kě)以成功地完成中(zhōng)風後腦損傷修複的細胞治療,包括成體(tǐ)幹細胞、胚胎幹細胞或誘導多(duō)能(néng)幹細胞(iPSCs)。然而,所有(yǒu)類型的細胞在其适用(yòng)性方面都存在局限性。未來仍然需要更多(duō)的研究探索以解決局限性。
臨床上,最常用(yòng)的成體(tǐ)幹細胞來源是間充質(zhì)幹細胞,因為(wèi)它們易于獲得和分(fēn)離。間充質(zhì)幹細胞可(kě)提供營養支持,但不能(néng)分(fēn)化為(wèi)神經譜系;間充質(zhì)幹細胞主要發揮着旁分(fēn)泌作(zuò)用(yòng)及營養支持作(zuò)用(yòng)。

與成體(tǐ)幹細胞相比,胚胎幹細胞具(jù)有(yǒu)更強的分(fēn)化為(wèi)多(duō)種細胞類型的能(néng)力,并且可(kě)以無限增殖。然而,它們的應用(yòng)受到嚴重的倫理(lǐ)問題的限制,而且他(tā)們有(yǒu)更高的緻瘤風險。
随着誘導多(duō)能(néng)幹細胞(iPSCs)的引入,倫理(lǐ)方面的擔憂得到了克服。iPSCs是通過将體(tǐ)細胞重編程為(wèi)多(duō)能(néng)胚胎幹細胞樣狀态而産(chǎn)生的,在移植之前,iPSCs通常被分(fēn)化成所需的神經細胞類型,并通過增殖再移植到特定大腦部位以促進大腦再生[1]。
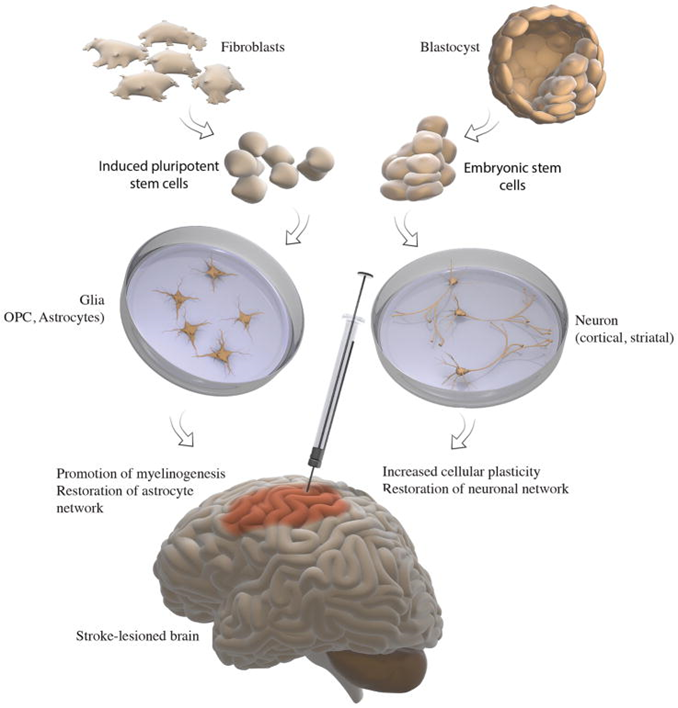
圖片來自文(wén)獻[3]
02 細胞移植途徑
如何保證移植細胞最大化到達及定植于受損大腦,這是目前有(yǒu)待探讨的一大問題,盡管臨床前的細胞治療研究傾向于腦内局部移植,但超過一半的臨床試驗更傾向于通過血管注射來移植細胞。
該領域面臨着一個兩難境地:腦内局部細胞移植有(yǒu)望實現最大療效,但注射的相關風險阻礙了其廣泛應用(yòng)。此外,血管注射是微創的;然而,大多(duō)數細胞最終進入了非靶器官,因此治療效果大打折扣。同時,根據移植細胞類型、腦損傷的時間和嚴重程度以及相關的血腦屏障損傷等,到達受損大腦的細胞數量也有(yǒu)所差異。
為(wèi)了提高移植幹細胞的靶向富集及駐留,研究人員開發了多(duō)種聯合手段,如在局部注射時,利用(yòng)水凝膠包裹移植細胞群,這種方法增強了移植物(wù)的駐留力和存活率,同時改善了移植物(wù)的成熟度;此外,在全身注射時,可(kě)仿照嵌合抗原受體(tǐ)T細胞(CAR-T)治療癌症的原理(lǐ),在移植細胞表面裝(zhuāng)飾上可(kě)靶向卒中(zhōng)相關多(duō)肽的抗體(tǐ),可(kě)能(néng)會增強移植物(wù)在損傷部位的歸巢,并在全身應用(yòng)後提供更有(yǒu)針對性和更有(yǒu)效的細胞治療[1]。
03 細胞移植時機
中(zhōng)風後腦組織在急性期形成一個有(yǒu)害的環境,具(jù)有(yǒu)高水平的炎症、氧化應激、細胞死亡和碎片,這降低了移植細胞的存活機會。因此,為(wèi)了避免上述有(yǒu)害環境,細胞治療的最佳治療窗口估計是在卒中(zhōng)後幾天至1周,以确保移植細胞的長(cháng)期存活。對于全身移植來說,這一時間點的血腦屏障通透性降低,更有(yǒu)利于移植細胞到達受損部位[1]。

同時,目前對于幹細胞在中(zhōng)風後不同時間點的作(zuò)用(yòng)機制也有(yǒu)了初步探索,在中(zhōng)風後的急性期和亞急性期,幹細胞治療主要通過直接替代和分(fēn)泌營養因子以促進功能(néng)恢複。在慢性期,幹細胞的支持作(zuò)用(yòng)可(kě)能(néng)是主要的治療機制。
04 免疫相容性
免疫排斥是細胞治療中(zhōng)的另一個關鍵問題。自體(tǐ)iPSC療法(即使用(yòng)從患者自身體(tǐ)細胞産(chǎn)生的iPSCs)可(kě)能(néng)是繞過這一問題的最合适的選擇,然而,由于生産(chǎn)個體(tǐ)化iPSCs費時,費力,費錢,嚴重限制了其臨床應用(yòng)及用(yòng)于急性疾病的治療。
因此,科(kē)學(xué)家們嘗試能(néng)否開發出具(jù)有(yǒu)最高免疫相容性的同種異體(tǐ)iPSCs,這樣便可(kě)以實現iPSCs的商(shāng)品化應用(yòng)。目前,已經針對在免疫排斥中(zhōng)發揮關鍵作(zuò)用(yòng)的人白細胞抗原 (HLA) 進行基因改造,以便讓細胞移植的同種異體(tǐ)應用(yòng)早日克服免疫相容性問題。
此外,間充質(zhì)幹細胞具(jù)有(yǒu)低免疫原性的有(yǒu)點,目前在多(duō)個臨床試驗中(zhōng)被采用(yòng),同種異體(tǐ)使用(yòng)時無需配型[4]。在臨床上具(jù)有(yǒu)十分(fēn)廣闊的前景。
05 風險最小(xiǎo)化
任何一項醫(yī)療技(jì )術都存在風險,更何況将活的細胞注射到大腦中(zhōng),風險包括急性腦出血(在立體(tǐ)定向局部注射時)、細胞凝結或細胞誘導的血管栓塞(在全身注射時)以及功能(néng)性副作(zuò)用(yòng)(如癫痫發作(zuò)和不自主運動)。從長(cháng)遠(yuǎn)方面來看,最大的擔憂是移植細胞形成惡性腫瘤以及移植細胞的非靶向富集。對于成體(tǐ)幹細胞而言,盡管間充質(zhì)幹細胞治療的安(ān)全性已經在多(duō)個臨床研究中(zhōng)被證實,未來仍然需要開展更大規模的研究。
因此,為(wèi)了實現風險的最小(xiǎo)化,必須對質(zhì)量控制、分(fēn)化方案、注射細胞數量和注射途徑等進行深入探索,并建立規範化流程。
中(zhōng)風的細胞治療在可(kě)預見的未來有(yǒu)巨大的潛力,為(wèi)患者提供一種保命及功能(néng)恢複的手段。目前正在開發遺傳和藥理(lǐ)學(xué)工(gōng)具(jù),以确保移植細胞精(jīng)确定位到大腦受損區(qū)域。總之,中(zhōng)風的細胞療法前途無限,但仍需開拓!
參考文(wén)獻:
[1] Rust R, Tackenberg C. Stem Cell Therapy for Repair of the Injured Brain: Five Principles [published online ahead of print, 2022 Aug 13]. Neuroscientist. 2022;10738584221110100.
https://pubmed.ncbi.nlm.nih.gov/35968796/
[2] Feigin VL, Brainin M, Norrving B, et al. World Stroke Organization (WSO): Global Stroke Fact Sheet 2022 [published correction appears in Int J Stroke. 2022 Apr;17(4):478]. Int J Stroke. 2022;17(1):18-29.
https://pubmed.ncbi.nlm.nih.gov/34986727/
[3] Kokaia Z, Llorente IL, Carmichael ST. Customized Brain Cells for Stroke Patients Using Pluripotent Stem Cells. Stroke. 2018;49(5):1091-1098.
https://pubmed.ncbi.nlm.nih.gov/29669871/
[4] Macías-Sánchez MDM, Morata-Tarifa C, Cuende N, et al. Mesenchymal Stromal Cells for Treating Steroid-Resistant Acute and Chronic Graft Versus Host Disease: A Multicenter Compassionate Use
Experience [published online ahead of print, 2022 Mar 28]. Stem Cells Transl Med. 2022;szac003.
https://pubmed.ncbi.nlm.nih.gov/35348788/
複制本文(wén)鏈接 文(wén)章為(wèi)作(zuò)者獨立觀點不代表本網站立場,未經允許不得轉載。

 京公(gōng)網安(ān)備
11010802036058号
京公(gōng)網安(ān)備
11010802036058号
評論