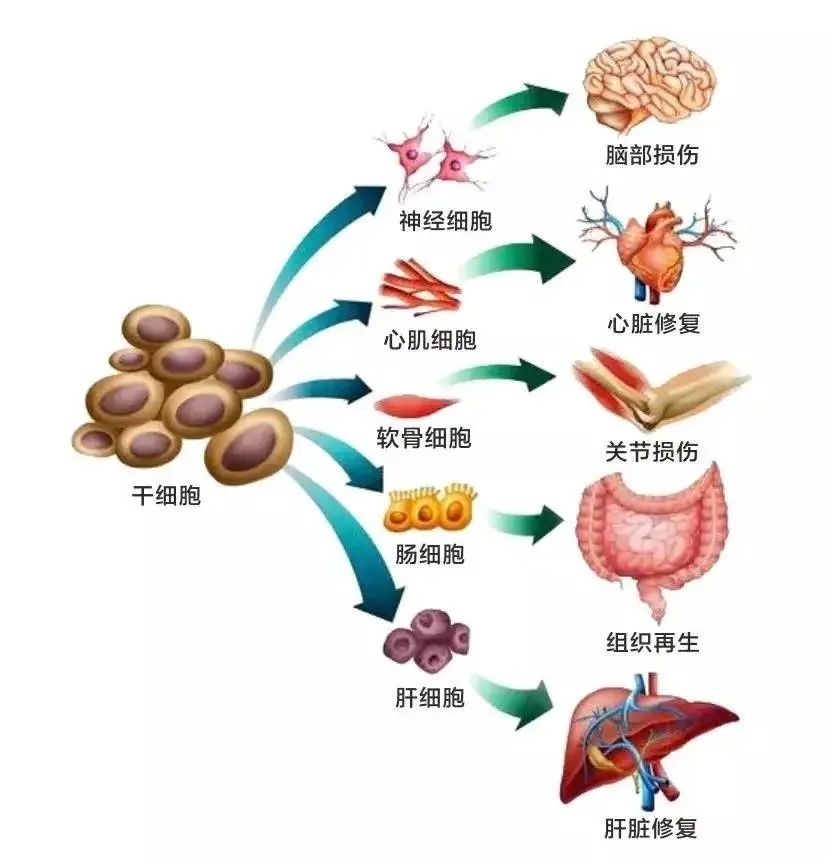
醫(yī)學(xué)治療方案中(zhōng)幹細胞方法是最前沿、最熱門的方向之一,取得了世人矚目的成果。我們現在了解到的成功的臨床試驗,每一次背後都有(yǒu)紮實的基礎研究,其中(zhōng)涉及幹細胞本身的生物(wù)學(xué)特性、适應症的選擇,給藥方式的選擇,細胞的選擇和給藥的劑量,都是成功的要素。現在政府政策大力鼓勵和支持,将有(yǒu)效規範和推動幹細胞産(chǎn)業的發展。
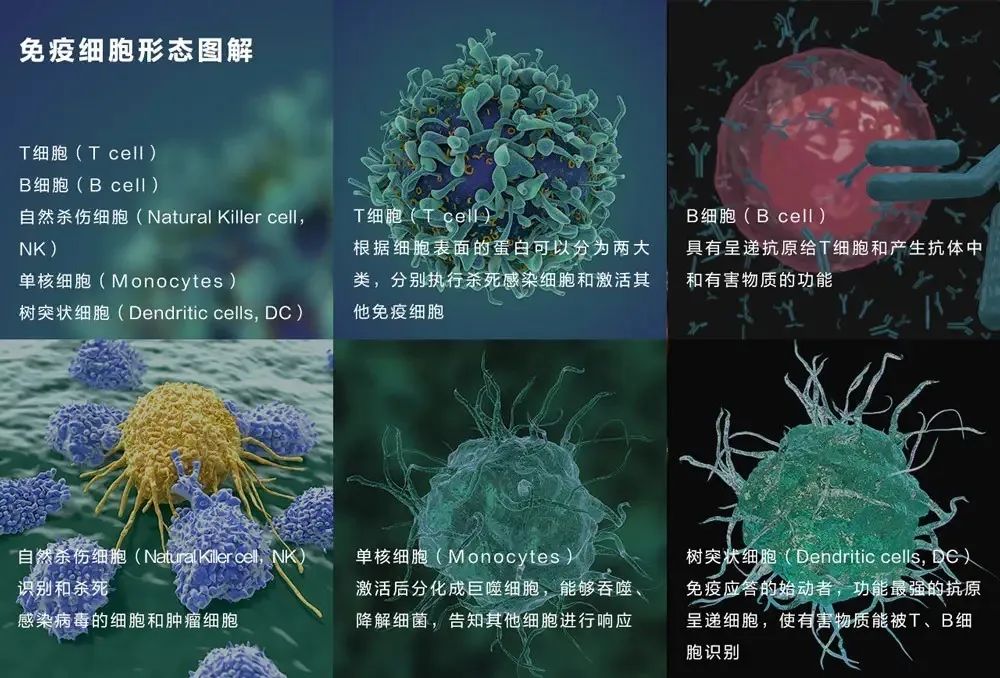
我們将從藥物(wù)治療過渡到二十一世紀的細胞治療。

上一個世紀的治療方法主要是化學(xué)藥物(wù),在遇到一些複雜的疾病時往往捉襟見肘,幹細胞治療方法在帕金森氏綜合症、老年癡呆症、糖尿病、肝纖維化、白血病、抗衰老等多(duō)種領域均有(yǒu)顯著療效,臨床醫(yī)學(xué)的數據證明了這些療效的一緻性和可(kě)靠性。未來幹細胞研究成果将覆蓋更多(duō)疑難雜症,造福社會,引領全新(xīn)的再生醫(yī)學(xué)革命。

2022年兩會
近年來幹細胞已成為(wèi)研機構和企業競相研究的熱點,各國(guó)政府也紛紛将幹細胞研究及應用(yòng)列為(wèi)國(guó)家重點發展的産(chǎn)業。2022年兩會陸續開幕,北京、湖(hú)南、大連等地關于細胞治療産(chǎn)業的發展備受關注,而在今年這個特殊時期,更是受到民(mín)衆的期待。細胞治療進入2022年各地兩會議題,北京政府報告:加快新(xīn)型細胞治療、基因編輯等生物(wù)前沿技(jì )術轉化應用(yòng)
2022年1月6日在北京市第十五屆人民(mín)代表大會第五次會議上

北京市市長(cháng)陳吉甯
2022年1月6日,北京市第十五屆人大五次會議在北京會議中(zhōng)心開幕。北京市市長(cháng)陳吉甯在市人民(mín)政府工(gōng)作(zuò)報告中(zhōng)提出:進一步做強新(xīn)一代信息技(jì )術、醫(yī)藥健康“雙引擎”,推動集成電(diàn)路、人工(gōng)智能(néng)、通信等領域“卡脖子”技(jì )術實現新(xīn)突破,加快新(xīn)型細胞治療、基因編輯等生物(wù)前沿技(jì )術突破和轉化應用(yòng),加速創新(xīn)藥、高端醫(yī)療器械産(chǎn)業化進程。
湖(hú)南:政協委員支持湖(hú)南幹細胞與再生醫(yī)學(xué)産(chǎn)業集群發展

湖(hú)南省政協委員吳金明、孔和平、陳宏忠、鄭安(ān)生聯名(míng)建議湖(hú)南參照天津、深圳等地做法,特許自貿區(qū)内的臨床機構開展幹細胞治療臨床應用(yòng)以及成本性收費,以吸引全國(guó)幹細胞技(jì )術及備案企業在園區(qū)聚集,形成虹吸效應,加速科(kē)研項目落地、轉化、孵化以及産(chǎn)業化,促進湖(hú)南省幹細胞與再生醫(yī)學(xué)産(chǎn)業集群發展。建議省藥監局及相關主管部門成立專門藥物(wù)申報專項工(gōng)作(zuò)組,按照省内幹細胞與再生醫(yī)學(xué)戰略性新(xīn)興産(chǎn)業集群龍頭企業的标準,支持幹細胞公(gōng)司快速進行幹細胞藥物(wù)申報,填補湖(hú)南省甚至國(guó)内國(guó)家一類生物(wù)創新(xīn)藥的空白。
遼甯大連:發力“幹細胞”打造完整産(chǎn)業鏈

目前,北京、深圳等地都瞄準細胞和基因等重大前沿産(chǎn)業領域發力。市人大代表劉晶建議大連發揮現有(yǒu)的技(jì )術、人才及高端研究平台等優勢,加速科(kē)技(jì )成果轉化,打造一條“幹細胞存儲-研發-應用(yòng)”的完整産(chǎn)業鏈。大連作(zuò)為(wèi)遼甯三大生物(wù)産(chǎn)業集聚區(qū)之一,現已初步形成了差異化、有(yǒu)特色的醫(yī)藥+醫(yī)療兩大集群,在幹細胞、中(zhōng)醫(yī)藥、基因檢測等方面積累了豐富的核心技(jì )術和大量的專業人才,建立了國(guó)家級幹細胞臨床研究機構、基因檢測示範中(zhōng)心、國(guó)際合作(zuò)基地等高端研究平台,形成了較好的産(chǎn)業應用(yòng)基礎。
黑龍江:做好幹細胞技(jì )術研究及産(chǎn)業化大文(wén)章
黑龍江省政府工(gōng)作(zuò)報告提出,加快培育壯大新(xīn)動能(néng)。對此,省人大代表王春梅呼籲,依托我省擁有(yǒu)的中(zhōng)國(guó)老年性疾病幹細胞工(gōng)程技(jì )術中(zhōng)心、東北地區(qū)臨床級别細胞制備中(zhōng)心等高科(kē)技(jì )研發平台,推動生命科(kē)學(xué)及産(chǎn)業化發展。
王春梅代表結合工(gōng)作(zuò)實際談到,幹細胞技(jì )術及産(chǎn)業化發展已列入國(guó)家重大科(kē)技(jì )發展戰略,預計到2020年全球幹細胞醫(yī)療的潛在市場規模将達到1745億美元。中(zhōng)國(guó)幹細胞産(chǎn)業為(wèi)世界第二,預計到2020年規模達到1200億人民(mín)币。與此相對應的是,我省幹細胞研究産(chǎn)業尚不具(jù)規模。如果我省在生命科(kē)學(xué)領域落後,未來大健康産(chǎn)業的發展就沒有(yǒu)後勁兒,也難以形成産(chǎn)業規模。
王春梅代表建議:把幹細胞研究和産(chǎn)業發展列入我省重大科(kē)技(jì )專項,建立幹細胞研究共享中(zhōng)心,建設示範基地,組建幹細胞技(jì )術研究院,搭建省級幹細胞學(xué)術研究平台,構建協調創新(xīn)機制,提升幹細胞臨床研究及轉化應用(yòng)能(néng)力和水平。設立引導資金,拓寬融資渠道,先行支持我省幹細胞産(chǎn)業領軍企業的發展(2022年1月14日黑龍江日報)。
全球幹細胞臨床研究項目超6000多(duō)項
幹細胞療法又(yòu)稱為(wèi)再生醫(yī)療技(jì )術,是指利用(yòng)幹細胞或其衍生的細胞,以特殊技(jì )術移植到體(tǐ)内,取代病人受損的細胞或通過招募内源性組織特異性幹細胞進而産(chǎn)生新(xīn)的組織,或發揮積極的免疫調節作(zuò)用(yòng)。通過再生醫(yī)學(xué),人體(tǐ)希望有(yǒu)一天能(néng)夠修複和恢複嚴重的組織損傷,甚至更換整個器官。
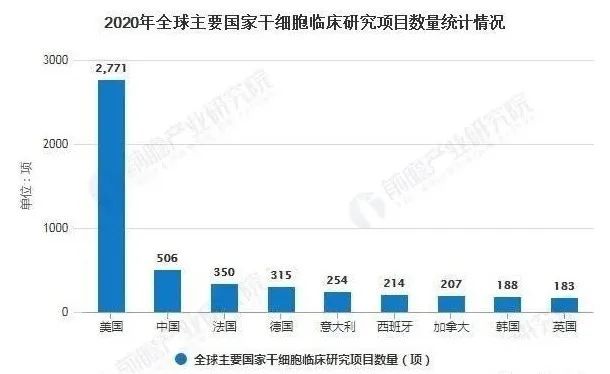
根據美國(guó)國(guó)立衛生研究院管理(lǐ)的臨床研究登記系統(Clinicaltrials.gov)數據顯示,截至2022年1月4日,全球登記的幹細胞臨床研究項目共計6065項,涉及糖尿病、骨關節炎、卒中(zhōng)、帕金森和脊柱損傷、血液系統疾病、神經系統疾病、肢體(tǐ)缺血性疾病、心腦血管疾病、分(fēn)泌系統疾病、外科(kē)疾病、皮膚病、腫瘤和免疫系統等上百種疾病。
其中(zhōng)美國(guó)保持絕對領先的地位,美國(guó)幹細胞臨床研究項目數量達到2865項,中(zhōng)國(guó)、法國(guó)和德(dé)國(guó)的幹細胞臨床研究項目數量分(fēn)别為(wèi)659項、378項和329項。截至2021年12月,全球已經有(yǒu)21款幹細胞産(chǎn)品獲批上市,分(fēn)布于美國(guó)、歐盟、韓國(guó)、加拿(ná)大、澳大利亞和日本等地。
前景廣闊!國(guó)家政策大力支持細胞治療産(chǎn)業發展

“十四五”時期以來,政策紅利繼續加持。2021年初國(guó)家重點研發計劃“十四五”總體(tǐ)布局形成,将“幹細胞研究與器官修複”納入“十四五”第一批啓動國(guó)家研發計劃的6個重點專項,持續促進幹細胞研究的規範和臨床應用(yòng)的轉化。
2021年,科(kē)技(jì )部《關于發布國(guó)家重點研發計劃“幹細胞研究與器官修複”等“十四五” 重點專項2021年度項目申報指南的通知》,2021年度指南圍繞幹細胞命運調控、基于幹細胞的發育和衰老研究、人和哺乳類器官組織原位再生、複雜器官制造與功能(néng)重塑、疾病的幹細胞、類器官與人源化動物(wù)模型等5個重點任務(wù)進行部署,拟支持17個項目,拟安(ān)排國(guó)撥經費概算4.4億元。同時,拟支持12個青年科(kē)學(xué)家項目,拟安(ān)排國(guó)撥經費概算6000萬元,每個項目500萬元。
2022年新(xīn)年伊始,國(guó)家科(kē)技(jì )管理(lǐ)信息系統公(gōng)共服務(wù)平台發布一批關于“國(guó)家重點研發計劃”重點專項項目的政策文(wén)件。對2021年度“十四五”國(guó)家重點研發計劃重點專項立項進行了公(gōng)示。北京大學(xué)等30個項目入選,國(guó)家撥款5億元,用(yòng)于支持重點研發"幹細胞研究與器官修複"重點專項。
“幹細胞研究與器官修複”重點專項的申報将為(wèi)重要組織器官修複與替代及重大疾病診療提供了創新(xīn)理(lǐ)論和技(jì )術支持,讓幹細胞治療在臨床合理(lǐ)性、科(kē)學(xué)性、先進性上聽取各方意見和建議,有(yǒu)助于推動幹細胞技(jì )術的發展,也是幹細胞推進臨床的重要一步。相信有(yǒu)了政策的助推,不斷創新(xīn)的技(jì )術發展和越來越完善的規範制度,會讓幹細胞産(chǎn)業在我國(guó)飛速發展。
根據國(guó)家藥品監督管理(lǐ)局藥品審評中(zhōng)心(CDE)公(gōng)示信息顯示,截止2022年2月26日,我國(guó)共有(yǒu)26個幹細胞新(xīn)藥項目獲得國(guó)家臨床默示許可(kě)。分(fēn)别是胎盤、臍帶、骨髓、牙髓、宮血、異體(tǐ)/自體(tǐ)脂肪來源的間充質(zhì)幹細胞,适應證包括了膝骨關節炎、類風濕關節炎、糖尿病足潰瘍、肺纖維化、肝衰竭、卒中(zhōng)、急性呼吸窘迫綜合征、牙周炎、克羅恩病和GvHD等。截至2021年11月,幹細胞臨床研究備案項目達到111個,幹細胞臨床研究備案機構133家(含軍隊醫(yī)院)。
2021年,複星凱特的阿基侖賽注射液和藥明巨諾的瑞基奧侖賽注射液相繼獲批,中(zhōng)國(guó)迎來兩款商(shāng)業化CAR-T産(chǎn)品。細胞治療在國(guó)内邁入商(shāng)業化時代,生物(wù)技(jì )術公(gōng)司也争相布局細胞治療産(chǎn)業。


2022年1月,藥品生産(chǎn)質(zhì)量管理(lǐ)規範細胞質(zhì)量産(chǎn)品附錄(征求意見稿)發布了,全文(wén)11章53條,征求意見1個月,截止2022年2月。征求意見稿從人員、廠房與設施、供者及供者材料管理(lǐ)、物(wù)料與産(chǎn)品、生産(chǎn)管理(lǐ)、質(zhì)量管理(lǐ)、産(chǎn)品追溯系統等七個方面制定細胞治療産(chǎn)品規範。新(xīn)版GMP細胞治療産(chǎn)品附錄發布,行業健康發展非常有(yǒu)利。
新(xīn)版GMP細胞治療産(chǎn)品附錄以外,近些年國(guó)内還發布過部分(fēn)針對幹細胞或細胞治療産(chǎn)品的部分(fēn)法規,例如《人體(tǐ)細胞治療研究和制劑質(zhì)量控制技(jì )術指導原則》(2003,CDE),《幹細胞制劑質(zhì)量控制及臨床前研究指導原則(試行)》(2015,衛計委,食藥監局),《細胞治療産(chǎn)品研究與評價技(jì )術指導原則(試行)》(2016,CDE),《CAR-T細胞治療産(chǎn)品質(zhì)量控制檢測研究及非臨床研究考慮要點》(2018,中(zhōng)檢院),《細胞治療産(chǎn)品申請臨床試驗藥學(xué)研究和申報資料的考慮要點》(2018,CDE)等。政策和法規的完善推動了幹細胞行業的良性發展。
我們國(guó)内神經系統、心血管、腫瘤等患病衆多(duō),醫(yī)療需求有(yǒu)很(hěn)大拓展空間。細胞治療作(zuò)為(wèi)一種新(xīn)的前沿科(kē)技(jì )手段,可(kě)以為(wèi)各類複雜疾病帶來希望,新(xīn)技(jì )術的不斷開發和實踐,臨床研究不斷深入進行,未來細胞治療的空間大有(yǒu)可(kě)為(wèi)。
複制本文(wén)鏈接 文(wén)章為(wèi)作(zuò)者獨立觀點不代表本網站立場,未經允許不得轉載。

 京公(gōng)網安(ān)備
11010802036058号
京公(gōng)網安(ān)備
11010802036058号
評論