基因治療或基因療法(英語:gene therapy)是利用(yòng)分(fēn)子生物(wù)學(xué)方法将目的基因導入患者體(tǐ)内,使之達成目的基因産(chǎn)物(wù),從而使疾病得到治療,為(wèi)現代醫(yī)學(xué)和分(fēn)子生物(wù)學(xué)相結合而誕生的新(xīn)技(jì )術。基因治療作(zuò)為(wèi)疾病治療的新(xīn)手段,它已有(yǒu)一些成功的應用(yòng),并且科(kē)學(xué)突破将繼續推動基因治療向主流醫(yī)療發展。
科(kē)學(xué)家嘗試将基因直接植入人體(tǐ)細胞中(zhōng),其中(zhōng),重點關注一些由單基因缺陷引起的疾病,如囊腫性纖維化,血友病,肌肉萎縮症和鐮狀細胞性貧血。不過,由于攜帶大段DNA并将其置入基因組的正确的位置非常困難,這種技(jì )術沒有(yǒu)得到普及。今天,大多(duō)數的基因治療研究的目的都是彌補癌症和遺傳疾病的基因缺陷或丢失。
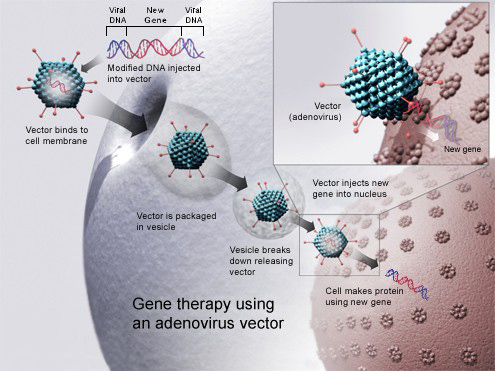
基因治療用(yòng)腺病毒載體(tǐ)。使用(yòng)腺病毒的新(xīn)基因插入細胞。如果治療是成功的,新(xīn)的基因,将産(chǎn)生功能(néng)性蛋白來治療疾病。
科(kē)學(xué)家曾嘗試用(yòng)此方法去治療一種叫嚴重免疫缺陷綜合征(Severe Combined Immunodeficiency, SCID)的疾病,并得到一定的成果。基本原理(lǐ)是用(yòng)已經被馴化了的病毒攜帶健康的基因,植入病人的細胞裏,以此去修補本身有(yǒu)缺陷的基因。
應用(yòng)腫瘤抑制基因(抑癌基因),對癌症進行靶向治療,是基因治療領域裏重要的研究項目。目前應用(yòng)較多(duō)的是p53抑瘤蛋白基因。
類型
種系基因療法
在種系基因治療的情況下,生殖細胞,即精(jīng)子或卵子,通常依據功能(néng)基因被修改整合進入基因組中(zhōng)。因此,這種通過治療後的改變可(kě)以遺傳且能(néng)傳給後代。這種新(xīn)的方法,從理(lǐ)論上說,應該會對基因性疾病和遺傳性疾病的對抗非常有(yǒu)效。然而,因為(wèi)種種技(jì )術與倫理(lǐ)問題,許多(duō)司法管轄區(qū)禁止在人類身上應用(yòng)這一治療手段 。
體(tǐ)細胞基因治療(Somatic gene therapy)
在體(tǐ)細胞基因治療的情況下,治療基因轉移到病人的體(tǐ)細胞。任何基因的修改和産(chǎn)生的效果将隻體(tǐ)現在接受治療的病人身上,并不會被病人的子女或後人繼承,這主要與體(tǐ)細胞的性質(zhì)與功能(néng)有(yǒu)關。
載體(tǐ)
病毒載體(tǐ)
病毒會與他(tā)們的宿主細胞結合,引入它們的遺傳物(wù)質(zhì)作(zuò)為(wèi)其宿主細胞複制循環的一部分(fēn)。這種遺傳物(wù)質(zhì)包含病毒的基本信息,比如如何産(chǎn)生這些病毒的副本,如何破壞人體(tǐ)的正常生産(chǎn)機制以滿足該病毒的需要。宿主細胞将執行這些指令并産(chǎn)生更多(duō)的病毒副本,以至于越來越多(duō)的正常細胞将受到感染。某些類型的病毒将自己的基因插入到宿主的基因組,但自己并不進入細胞;還有(yǒu)的病毒可(kě)以僞裝(zhuāng)成蛋白質(zhì)分(fēn)子穿透細胞膜進入細胞(例如腺病毒會被内吞到内體(tǐ)複合體(tǐ)從而進入細胞)。 病毒有(yǒu)兩種類型的轉化:裂解和溶源。裂解性病毒DNA插入後不久,在該病毒生長(cháng)期中(zhōng)的裂解期,細胞裂解液中(zhōng)數目急劇增加的病毒會被釋放,感染更多(duō)的細胞。溶源性病毒整合自己的DNA到宿主細胞DNA中(zhōng),并可(kě)能(néng)在體(tǐ)内存活好幾年才爆發。該病毒感染的宿主細胞也并不會造成身體(tǐ)傷害,直到被觸發引起宿主細胞破裂,釋放宿主細胞DNA來産(chǎn)生新(xīn)的病毒。如SARS病毒和艾滋病毒就是溶源性病毒。一些科(kē)學(xué)家認為(wèi),如果他(tā)們找到其觸發來源,他(tā)們将能(néng)夠阻止整個身體(tǐ)不斷複制該病毒。
反轉錄病毒
反轉錄病毒的遺傳本質(zhì)是RNA分(fēn)子,而其宿主細胞的遺傳物(wù)質(zhì)是DNA。當反轉錄病毒感染宿主細胞,其RNA将與逆轉錄酶和整合酶共同作(zuò)用(yòng),從而進入細胞。這種病毒的RNA分(fēn)子必須反轉錄産(chǎn)生對應的DNA分(fēn)子,才能(néng)與宿主細胞的遺傳物(wù)質(zhì)相結合。這種由一個RNA分(fēn)子得到其對應DNA的過程稱為(wèi)反轉錄,反轉錄過程在病毒攜帶的逆轉錄酶作(zuò)用(yòng)下完成。此後,反轉錄産(chǎn)生的DNA必須納入宿主細胞DNA分(fēn)子中(zhōng),此過程在整合酶作(zuò)用(yòng)下進行。此時宿主細胞已包含病毒的遺傳物(wù)質(zhì),如果宿主細胞分(fēn)裂,其後代都将包含病毒的遺傳物(wù)質(zhì),但這些基因有(yǒu)時并不會及時表達。有(yǒu)時使用(yòng)反轉錄病毒進行基因治療會出現問題,整合酶會随機插入到宿主遺傳物(wù)質(zhì)中(zhōng)病毒基因組的任意位置,如果恰好在宿主細胞的一個正常基因的中(zhōng)間插入,正常基因将被破壞,稱為(wèi)插入突變;如果恰好插入的是調節細胞分(fēn)裂的基因,那麽插入後細胞分(fēn)裂失控,即癌症可(kě)能(néng)發生。譬如使用(yòng)逆轉錄病毒載體(tǐ)治療的10例X連鎖重度複合型免疫缺陷病(X-SCID),患者中(zhōng),有(yǒu)4例因載體(tǐ)整合在原癌基因LMO2等的附近,激活下遊基因的表達而罹患白血病。但此問題最近開始得到解決,比如利用(yòng)鋅指核酸酶技(jì )術在幹細胞的DNA的安(ān)全位點插入野生型珠蛋白基因,基因編輯後獲得的含正常β-珠蛋白基因的幹細胞分(fēn)化形成的紅細胞能(néng)表達正常的β-珠蛋白。。
腺病毒
腺病毒是以雙鏈DNA為(wèi)遺傳物(wù)質(zhì)的病毒。他(tā)們引起人類呼吸道、腸道、和眼睛感染(尤其是上呼吸道感染)。當這些病毒感染宿主細胞時,會将它們的DNA引入到宿主的DNA分(fēn)子中(zhōng)。腺病毒遺傳物(wù)質(zhì)DNA分(fēn)子在宿主細胞的核中(zhōng)自由存在,并像其他(tā)基因一樣轉錄。唯一不同的是,這些基因在細胞分(fēn)裂時不會複制,其後代細胞将不會有(yǒu)這種基因。這個載體(tǐ)系統已用(yòng)于治療癌症,并且第一個基因治療産(chǎn)品即用(yòng)于癌症的治療。腺病毒Gendicine是以p53基因的腺病毒為(wèi)基礎的基因療法,在2003年被中(zhōng)國(guó)食品監督局SFDA(現更名(míng)為(wèi)國(guó)家食品藥品監督管理(lǐ)總局CFDA)批準用(yòng)于治療頭頸部癌症。 關于腺病毒載體(tǐ)的擔憂在1999年傑西基辛格(Jesse Gelsinger)死後被提出來予以重視。從那時起,利用(yòng)腺病毒載體(tǐ)進行基因治療的工(gōng)作(zuò)重點便被放在病毒的遺傳學(xué)缺陷上。
腺相關病毒
腺相關病毒,來自于parvovirus病毒家族,是擁有(yǒu)單鏈DNA的基因組的小(xiǎo)型病毒。野生型腺相關病毒的遺傳物(wù)質(zhì)可(kě)以有(yǒu)近100%的準确性插入在19号染色體(tǐ)上的特定位點。但是,重組腺相關病毒,其中(zhōng)不包含任何病毒基因隻有(yǒu)治療基因,不整合到基因組中(zhōng)。相反,重組病毒在其兩端通過ITR(末端反向重複)重組基因融合,形成圓環式可(kě)表達的基因組。同時這種病毒的利用(yòng)也有(yǒu)一些缺點,其中(zhōng)包括可(kě)攜帶DNA及其少量(低容量),并且生産(chǎn)它存在難度。生産(chǎn)問題最近由Amsterdam Molecular Therapeutics得到解決。這類型的病毒正在使用(yòng)階段,但是,因為(wèi)它不具(jù)有(yǒu)緻病性(大多(duō)數人攜帶這種無害的病毒)。與腺病毒不同的是,與大多(duō)數腺相關病毒治療的人不會建立一種免疫應答(dá)來清除它。腺相關病毒的試驗仍在進行中(zhōng)或準備中(zhōng),主要是用(yòng)于治療肌肉和眼部疾病,病毒似乎對于這兩種組織特别有(yǒu)用(yòng)。然而,臨床試驗也已展開腺相關病毒載體(tǐ)用(yòng)于基因傳遞到大腦的實驗。這是很(hěn)可(kě)能(néng)的,因為(wèi)腺病毒能(néng)夠感染非分(fēn)裂(靜态)細胞,如它們的基因組中(zhōng)神經元長(cháng)時間表達。
病毒載體(tǐ)的蛋白質(zhì)包被的假型化
上述的病毒載體(tǐ)具(jù)有(yǒu)天然宿主的細胞群,他(tā)們感染最有(yǒu)效。逆轉錄病毒的天然宿主細胞的範圍有(yǒu)限,雖然腺病毒和腺相關病毒能(néng)夠有(yǒu)效感染相對範圍内的細胞,但某些細胞類型很(hěn)難控制并駕馭這些病毒體(tǐ)。進入易感細胞是由病毒表面的蛋白包膜介導的。逆轉錄病毒和腺相關病毒有(yǒu)一個單一的蛋白質(zhì)包被膜,而腺病毒有(yǒu)包膜蛋白和纖維共同交聯于病毒表面。對這些病毒的包膜蛋白結合到每個細胞表面分(fēn)子,如heparin sulfate,他(tā)們定位在潛在寄主的表面,像特定的蛋白質(zhì)受體(tǐ)一樣。進入潛在寄主需要宿主細胞表面蛋白與病毒表面蛋白很(hěn)好的相互作(zuò)用(yòng)。根據基因治療的目的,我們應該盡量控制細胞的易感性适中(zhōng)。為(wèi)此,許多(duō)載體(tǐ)發展到 内源性病毒包膜蛋白已被其他(tā)病毒包膜蛋白或嵌合體(tǐ)蛋白所取代。這種嵌合體(tǐ)包含病毒蛋白必須的部分(fēn),可(kě)以協同進入寄主并且與宿主細胞蛋白相互作(zuò)用(yòng)。其中(zhōng)包膜蛋白病毒已被描述成pseudotyped viruses。例如,最流行的基因治療試驗中(zhōng)使用(yòng)的逆轉錄病毒載體(tǐ)是lentivirusSimian免疫缺陷病毒包膜蛋白-G蛋白,來自Vesicular stomatitis virus。
順式反式作(zuò)用(yòng)元件
複制缺陷型載體(tǐ)始終包含一個“傳輸結構”。它攜帶那些對基因功能(néng)執行相關的基因序列,包裝(zhuāng)序列,複制和在必要時啓動反轉錄。這些均是順式作(zuò)用(yòng)元件。反式作(zuò)用(yòng)元件是病毒性的元素,它可(kě)以在不同的DNA分(fēn)子進行編碼。例如,病毒結構蛋白可(kě)以從不同的基因組元件進行表達。
單純疱疹病毒
單純疱疹病毒是一種人類嗜神經病毒。這主要是研究基因在神經系統的傳遞。野生型HSV - 1的病毒能(néng)夠感染細胞。受感染的神經元都沒有(yǒu)能(néng)夠對抗的免疫系統。雖然沒有(yǒu)轉錄病毒潛伏明顯,它具(jù)有(yǒu)神經元特異性啓動子,可(kě)以繼續正常工(gōng)作(zuò)。單純疱疹病毒抗體(tǐ)- 1比較常見,但疱疹病毒感染的并發症很(hěn)罕見。
非病毒方法
非病毒的方法比某些病毒方法更有(yǒu)優勢,因為(wèi)其大規模生産(chǎn)的簡單工(gōng)藝和低免疫原性。在此之前,轉染和基因表達水平低的缺點是非病毒基因治療十分(fēn)困難。然而,在載體(tǐ)技(jì )術的最新(xīn)進展下,這種手段與病毒式治療異曲同工(gōng)。
裸露DNA
這就是非病毒轉染的最簡單方法。臨床試驗已成功進行了一些裸露DNA質(zhì)體(tǐ)的肌肉注射,但是相比其他(tā)的轉染方法,其表達非常低。除了質(zhì)體(tǐ)實驗,naked PCR的試驗也有(yǒu)開展并取得一定的成功。這一成功為(wèi)更有(yǒu)效的方法提供可(kě)能(néng),諸如電(diàn)穿孔儀(electroporation), 聲孔作(zuò)用(yòng)(sonoporation),還有(yǒu)基因槍的應用(yòng),其中(zhōng)利用(yòng)高壓氣體(tǐ)擊中(zhōng)包覆DNA的金粒子進入細胞.
寡核苷酸
合成的寡核苷酸的用(yòng)途是滅活疾病過程有(yǒu)關的基因。其中(zhōng)有(yǒu)幾種方法達到這一目的。将目的基因antisense達到破壞基因轉錄的目的。另一種小(xiǎo)分(fēn)子RNA稱siRNA,利用(yòng)它來标記細胞,在mRNAh缺陷基因轉錄中(zhōng)分(fēn)開特定的序列,從而打斷缺陷mRNA的表達,即基因的表達。還有(yǒu)一種更優方法,使用(yòng)雙鏈寡核苷酸作(zuò)為(wèi)轉錄因子激活靶基因的轉錄。轉錄因子結合,而不是有(yǒu)缺陷的基因,從而降低了目的基因的轉錄,降低表達。此外,單鏈寡核苷酸DNA已被用(yòng)來指導一個突變基因的單堿基改變。寡核苷酸介導的基因修複,有(yǒu)針對性的基因修複,或有(yǒu)針對性的核苷酸改變成為(wèi)熱點。
Lipoplexes and polyplexes
為(wèi)了提高新(xīn)的DNA進入細胞内,DNA必須得到保護,免受損害,其進入細胞必須提供便利。為(wèi)此新(xīn)的分(fēn)子lipoplexes和polyplexes,已經成功創建,有(yǒu)能(néng)力保護降解過程中(zhōng)的DNA轉染。質(zhì)體(tǐ)DNA可(kě)包被脂質(zhì),形态有(yǒu)膠束或脂質(zhì)體(tǐ)。當結構物(wù)質(zhì)複合DNA的成為(wèi)lipoplex。有(yǒu)三種類型的脂質(zhì),陰離子(負電(diàn)荷),中(zhōng)性,或陽離子(帶正電(diàn))。起初,陰離子和中(zhōng)性脂質(zhì)被用(yòng)于建立lipoplexes來合成載體(tǐ)。然而,在事實的,很(hěn)少有(yǒu)與他(tā)們相關的毒性,它們與體(tǐ)液兼容,但根據組織特異性可(kě)适應也有(yǒu)可(kě)能(néng),陽離子脂質(zhì),由于其正電(diàn)荷,首次使用(yòng)帶負電(diàn)荷的DNA分(fēn)子凝聚,以促進脂質(zhì)體(tǐ)DNA導入的封裝(zhuāng)。後來人們發現,利用(yòng)陽離子脂質(zhì)顯著提高了lipoplexes穩定。另外由于他(tā)們負責的結果,陽離子脂質(zhì)體(tǐ)與細胞膜相互作(zuò)用(yòng),内吞作(zuò)用(yòng)被廣泛認為(wèi)是主要路線(xiàn),使細胞吸收lipoplexes。内涵體(tǐ)的形成,作(zuò)為(wèi)内吞作(zuò)用(yòng)的結果,但是,如果破壞細胞質(zhì)内體(tǐ)膜釋放基因仍不能(néng)成功,它們将被溶酶體(tǐ)消化。有(yǒu)人還發現,雖然可(kě)以濃縮陽離子脂質(zhì)和脂質(zhì)體(tǐ)封裝(zhuāng)到的DNA,但由于能(néng)力在“内體(tǐ)逃離”方面的不足,轉染效率非常低。然而,當助手脂類(通常電(diàn)中(zhōng)性脂肪,如塗料,)分(fēn)别加入,形成lipoplexes,可(kě)以觀察到更高的轉染效率。後來,有(yǒu)人想出了某些脂類有(yǒu)能(néng)力颠覆内體(tǐ)膜,以便DNA逃脫從内體(tǐ),因此那些被稱為(wèi)脂質(zhì)膜融合脂質(zhì)。雖然陽離子脂質(zhì)體(tǐ)載體(tǐ)已被廣泛用(yòng)作(zuò)傳遞一種替代基因,陽離子脂質(zhì)劑量依賴性毒性也可(kě)能(néng)會限制他(tā)們的治療用(yòng)途。lipoplexes的使用(yòng)最普遍的基因已經被轉移到癌細胞,其中(zhōng)所提供的基因在細胞中(zhōng)激活腫瘤抑制基因的控制,降低緻癌基因的活性。最近的研究表明lipoplexes可(kě)用(yòng)于治療遺傳性疾病如囊性纖維化呼吸。DNA複合物(wù)與聚合物(wù)被稱為(wèi)polyplexes。
混合方法
由于每一個基因轉移方法都是有(yǒu)缺陷的,開發有(yǒu)兩個或兩個以上相結合的混合方法的一些技(jì )術會更有(yǒu)效。 譬如Virosomesare結合脂質(zhì)體(tǐ)滅活艾滋病病毒或流感病毒,這已被證明具(jù)有(yǒu)更有(yǒu)效的轉移方法,位于呼吸道上皮細胞相比于比任何單獨的病毒或脂質(zhì)體(tǐ)。其他(tā)方法包括與orhybridising病毒混合陽離子脂質(zhì)與其他(tā)病毒載體(tǐ)。
複制本文(wén)鏈接 文(wén)章為(wèi)作(zuò)者獨立觀點不代表本網站立場,未經允許不得轉載。

 京公(gōng)網安(ān)備
11010802036058号
京公(gōng)網安(ān)備
11010802036058号
評論